ወቅታዊ የጠረጴዛ ምልክት. የዲአይ ሜንዴሌቭ የኬሚካል ንጥረ ነገሮች ወቅታዊ ስርዓት
የፔሪዲክ ሠንጠረዥን እንዴት መጠቀም እንደሚቻል ለማያውቅ ሰው ፣የፔርዲክቲክ ሰንጠረዡን ማንበብ የጥንቱን የኤልቭስ ሩጫዎች ለድዋፍ ከመመልከት ጋር ተመሳሳይ ነው። እና ወቅታዊው ሰንጠረዥ, በነገራችን ላይ, በትክክል ጥቅም ላይ ከዋለ, ስለ ዓለም ብዙ ሊናገር ይችላል. በፈተና ውስጥ እርስዎን ከማገልገል በተጨማሪ እጅግ በጣም ብዙ ኬሚካላዊ እና አካላዊ ችግሮችን ለመፍታት እንዲሁ በጣም አስፈላጊ ነው። ግን እንዴት ማንበብ ይቻላል? እንደ እድል ሆኖ, ዛሬ ሁሉም ሰው ይህን ጥበብ መማር ይችላል. በዚህ ጽሑፍ ውስጥ ወቅታዊውን ሰንጠረዥ እንዴት እንደሚረዱ እናነግርዎታለን.
የኬሚካል ንጥረ ነገሮች ወቅታዊ ስርዓት (የሜንዴሌቭ ሰንጠረዥ) በአቶሚክ አስኳል ክፍያ ላይ የተለያዩ የንጥረ ነገሮች ጥገኛ ጥገኛነትን የሚያረጋግጥ የኬሚካል ንጥረነገሮች ምደባ ነው።
የጠረጴዛው አፈጣጠር ታሪክ
ዲሚትሪ ኢቫኖቪች ሜንዴሌቭ ቀላል ኬሚስት አልነበረም, አንድ ሰው እንደዚያ ቢያስብ. እሱ ኬሚስት ፣ የፊዚክስ ሊቅ ፣ የጂኦሎጂስት ፣ የሜትሮሎጂስት ፣ የስነ-ምህዳር ባለሙያ ፣ ኢኮኖሚስት ፣ ዘይት ባለሙያ ፣ አየር ኖት ፣ መሳሪያ ሰሪ እና መምህር ነበር። ሳይንቲስቱ በህይወት ዘመናቸው በተለያዩ የእውቀት ዘርፎች ብዙ መሰረታዊ ምርምር ማድረግ ችለዋል። ለምሳሌ, የቮዲካ ተስማሚ ጥንካሬ - 40 ዲግሪዎች ያሰሉት ሜንዴሌቭቭ እንደሆነ በሰፊው ይታመናል. ሜንዴሌቭ ቮድካን እንዴት እንደያዘ አናውቅም ፣ ግን በእርግጠኝነት “በአልኮል መጠጥ ከውሃ ጋር ስለመጣመር ንግግር” በሚለው ርዕስ ላይ ያቀረበው የመመረቂያ ጽሑፍ ከቮድካ ጋር ምንም ግንኙነት እንደሌለው እና የአልኮሆል መጠን ከ 70 ዲግሪ እንደሆነ ተደርጎ እንደሚቆጠር በእርግጠኝነት ይታወቃል። በሁሉም የሳይንስ ሊቃውንት ጥቅሞች, የኬሚካል ንጥረ ነገሮች ወቅታዊ ህግን ማግኘቱ - ከተፈጥሮ መሠረታዊ ህግጋቶች አንዱ, ሰፊውን ዝና አመጣለት.

ሳይንቲስቱ ስለ ወቅታዊው ስርዓት ህልም ያዩበት አፈ ታሪክ አለ ፣ ከዚያ በኋላ የተፈጠረውን ሀሳብ ማጠናቀቅ ብቻ ነበረበት። ግን ፣ ሁሉም ነገር በጣም ቀላል ቢሆን .. ይህ የወቅቱ ሰንጠረዥ አፈጣጠር ስሪት ፣ እንደሚታየው ፣ ከአፈ ታሪክ ሌላ ምንም አይደለም። ዲሚትሪ ኢቫኖቪች ራሱ ጠረጴዛው እንዴት እንደተከፈተ ሲጠየቁ “ ስለ እሱ ምናልባት ለሃያ ዓመታት እያሰብኩ ነበር ፣ እና እርስዎ ያስባሉ-ተቀመጥኩ እና በድንገት… ዝግጁ ነው ።
በአስራ ዘጠነኛው ክፍለ ዘመን አጋማሽ ላይ የታወቁትን የኬሚካል ንጥረነገሮች (63 ንጥረ ነገሮች የታወቁ ነበሩ) ለማቀላጠፍ የተደረጉ ሙከራዎች በአንድ ጊዜ በበርካታ ሳይንቲስቶች ተካሂደዋል. ለምሳሌ፣ በ1862 አሌክሳንደር ኤሚሌ ቻንኮርቶስ ንጥረ ነገሮቹን በሄሊክስ ላይ በማስቀመጥ የኬሚካላዊ ባህሪያትን ዑደታዊ ድግግሞሽ አስተውሏል። ኬሚስት እና ሙዚቀኛ ጆን አሌክሳንደር ኒውላንድስ በ 1866 የወቅቱን ሰንጠረዥ እትም አቅርበዋል ። አንድ አስገራሚ እውነታ ሳይንቲስቱ በንጥረ ነገሮች ዝግጅት ውስጥ አንዳንድ ሚስጥራዊ የሙዚቃ ስምምነትን ለማግኘት ሞክረዋል ። ከሌሎች ሙከራዎች መካከል የስኬት ዘውድ የተቀዳጀው የሜንዴሌቭ ሙከራ አንዱ ነው።

በ 1869 የሠንጠረዡ የመጀመሪያ መርሃ ግብር ታትሟል, እና መጋቢት 1, 1869 የወቅቱ ህግ የተገኘበት ቀን ይቆጠራል. የሜንዴሌቭ ግኝት ፍሬ ነገር የአቶሚክ ብዛትን የሚጨምሩ ንጥረ ነገሮች ባህሪያቶች በአንድነት አይለወጡም ፣ ግን በየጊዜው። የሠንጠረዡ የመጀመሪያ ስሪት 63 አካላትን ብቻ ይዟል, ነገር ግን ሜንዴሌቭ በጣም ብዙ መደበኛ ያልሆኑ ውሳኔዎችን አድርጓል. ስለዚህ፣ በሠንጠረዡ ውስጥ ገና ላልተገኙ ንጥረ ነገሮች ቦታ እንደሚተው ገምቷል፣ እና የአንዳንድ ንጥረ ነገሮችን አቶሚክ ስብስቦችንም ለውጦታል። በሜንዴሌቭ የተገኘው የሕግ መሠረታዊ ትክክለኛነት ጋሊየም ፣ ስካንዲየም እና ጀርማኒየም ከተገኘ በኋላ ፣ ሕልውናው በሳይንቲስቶች ተንብየዋል ።
ወቅታዊ ሰንጠረዥ ወቅታዊ እይታ
ከታች ያለው ጠረጴዛው ራሱ ነው.
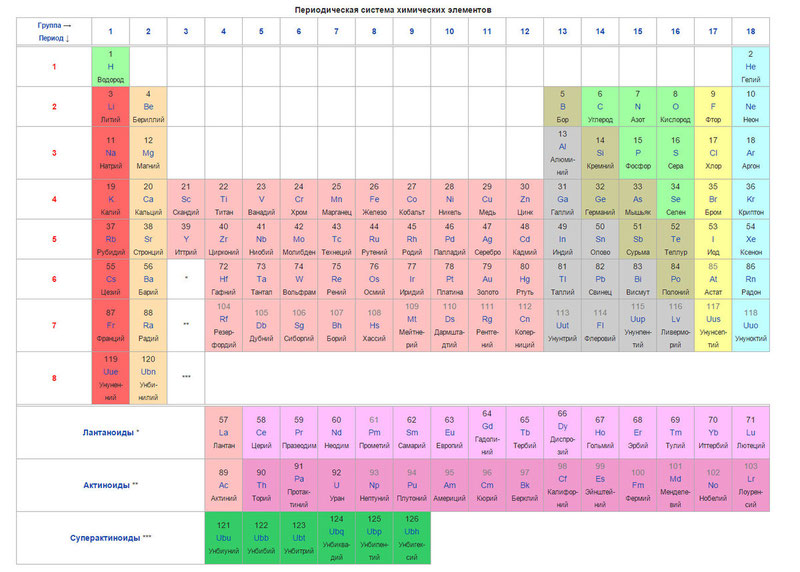
ዛሬ በአቶሚክ ክብደት (አቶሚክ ክብደት) ፋንታ የአቶሚክ ቁጥር ጽንሰ-ሐሳብ (በኒውክሊየስ ውስጥ ያሉ የፕሮቶኖች ብዛት) ንጥረ ነገሮችን ለማዘዝ ጥቅም ላይ ይውላል። ሠንጠረዡ 120 ንጥረ ነገሮችን ይዟል, እነሱም ከግራ ወደ ቀኝ ወደ ላይ በአቶሚክ ቁጥር (የፕሮቶን ብዛት) የተደረደሩ ናቸው.
የሠንጠረዡ ዓምዶች ቡድኖች ተብለው ይጠራሉ, እና ረድፎቹ ወቅቶች ናቸው. በሰንጠረዡ ውስጥ 18 ቡድኖች እና 8 ወቅቶች አሉ.
- ከግራ ወደ ቀኝ በሚንቀሳቀሱበት ጊዜ የንጥረ ነገሮች ብረታ ብረት ባህሪያት ይቀንሳሉ, እና በተቃራኒው አቅጣጫ ይጨምራሉ.
- በየወቅቱ ከግራ ወደ ቀኝ ሲንቀሳቀሱ የአተሞች መጠን ይቀንሳል።
- በቡድኑ ውስጥ ከላይ ወደ ታች ሲንቀሳቀሱ የሚቀነሱት የብረታ ብረት ባህሪያት ይጨምራሉ.
- ከግራ ወደ ቀኝ ባለው ጊዜ ውስጥ ኦክሳይድ እና ብረት ያልሆኑ ባህሪያት ይጨምራሉ.አይ.
ከጠረጴዛው ውስጥ ስላለው ንጥረ ነገር ምን እንማራለን? ለምሳሌ, በሠንጠረዡ ውስጥ ያለውን ሦስተኛውን ንጥረ ነገር - ሊቲየም እንውሰድ, እና በዝርዝር አስብበት.

በመጀመሪያ ደረጃ, የእራሱን ንጥረ ነገር ምልክት እና በእሱ ስር ያለውን ስም እናያለን. በላይኛው ግራ ጥግ ላይ የንጥሉ የአቶሚክ ቁጥር ነው, ኤለመንቱ በሠንጠረዡ ውስጥ በሚገኝበት ቅደም ተከተል. የአቶሚክ ቁጥር, ቀደም ሲል እንደተጠቀሰው, በኒውክሊየስ ውስጥ ከሚገኙት የፕሮቶኖች ብዛት ጋር እኩል ነው. የአዎንታዊ ፕሮቶኖች ብዛት በአብዛኛው በአተም ውስጥ ካሉት አሉታዊ ኤሌክትሮኖች ቁጥር ጋር እኩል ነው (ከ isotopes በስተቀር)።
የአቶሚክ ክብደት በአቶሚክ ቁጥር (በዚህ የሰንጠረዡ ስሪት) ስር ይገለጻል. የአቶሚክ ብዛትን ወደ ቅርብ ኢንቲጀር ካጠጋነው፣ የጅምላ ቁጥር የሚባለውን እናገኛለን። በጅምላ ቁጥር እና በአቶሚክ ቁጥር መካከል ያለው ልዩነት በኒውክሊየስ ውስጥ ያለውን የኒውትሮን ብዛት ይሰጣል። ስለዚህ, በሂሊየም ኒውክሊየስ ውስጥ የኒውትሮኖች ቁጥር ሁለት ነው, እና በሊቲየም - አራት.
ስለዚህ የእኛ ኮርስ "የሜንዴሌቭ ጠረጴዛ ለዳሚዎች" አብቅቷል. በማጠቃለያው, የቲማቲክ ቪዲዮን እንድትመለከቱ እንጋብዝዎታለን, እና የሜንዴሌቭን ወቅታዊ ሰንጠረዥ እንዴት እንደሚጠቀሙበት ጥያቄው ይበልጥ ግልጽ ሆኖልዎታል ብለን ተስፋ እናደርጋለን. አዲስ ትምህርት መማር ሁልጊዜ የበለጠ ውጤታማ ብቻውን ሳይሆን ልምድ ባለው አማካሪ እርዳታ እናስታውስዎታለን። ለዚህም ነው እውቀታቸውን እና ልምዳቸውን በደስታ ስለሚካፈሉ ሰዎች መቼም ቢሆን መርሳት የለብዎትም።
ኬሚካላዊ ንጥረ ነገር የአንድ ቀላል ንጥረ ነገር የአተሞች ስብስብን የሚገልጽ የጋራ ቃል ነው ፣ ማለትም ፣ ወደ ማንኛውም ቀላል (በሞለኪውሎቻቸው መዋቅር) ክፍሎች ሊከፋፈል የማይችል። በኬሚስቶች የተፈለሰፈውን ማንኛውንም መሳሪያ ወይም ዘዴ በመጠቀም ንፁህ ብረት ወደ መላምታዊ አካላት እንዲከፍሉ በመጠየቅ እንደተቀበሉ ያስቡ። ሆኖም ግን, ምንም ነገር ማድረግ አይችሉም, ብረቱ በጭራሽ ወደ ቀላል ነገር አይከፋፈልም. ቀላል ንጥረ ነገር - ብረት - ከኬሚካል ንጥረ ነገር Fe ጋር ይዛመዳል.
ቲዎሬቲካል ፍቺ
ከላይ የተመለከተው የሙከራ እውነታ የሚከተለውን ፍቺ በመጠቀም ሊገለጽ ይችላል፡- የኬሚካል ንጥረ ነገር የአተሞች ረቂቅ ስብስብ ነው (ሞለኪውሎች አይደሉም!) ተዛማጅ ቀላል ንጥረ ነገሮች ማለትም ተመሳሳይ ዓይነት አተሞች። ከላይ በተጠቀሰው የንፁህ ብረት ቁራጭ ውስጥ ያሉትን እያንዳንዱን አቶሞች የምንመለከትበት መንገድ ቢኖር ኖሮ ሁሉም አንድ ዓይነት ይሆናሉ - የብረት አተሞች። በአንጻሩ እንደ ብረት ኦክሳይድ ያለ የኬሚካል ውህድ ሁል ጊዜ ቢያንስ ሁለት የተለያዩ አይነት አቶሞችን ይይዛል፡- የብረት አተሞች እና የኦክስጂን አቶሞች።
ማወቅ ያለብዎት ውሎች
የአቶሚክ ክብደትየኬሚካል ንጥረ ነገር አቶም የሚሠሩት የፕሮቶን፣ ኒውትሮን እና ኤሌክትሮኖች ብዛት።
የአቶሚክ ቁጥርበአንድ ንጥረ ነገር አቶም ኒውክሊየስ ውስጥ ያሉ የፕሮቶኖች ብዛት።
የኬሚካል ምልክትየተሰጠውን አካል ስያሜ የሚወክል ፊደል ወይም ጥንድ የላቲን ፊደላት።
የኬሚካል ውህድሁለት ወይም ከዚያ በላይ ኬሚካላዊ ንጥረ ነገሮችን የያዘ ንጥረ ነገር በተወሰነ መጠን እርስ በርስ የተጣመሩ ናቸው.
ብረትከሌሎች ኤለመንቶች ጋር በሚፈጠር ኬሚካላዊ ምላሽ ኤሌክትሮኖችን የሚያጣ ንጥረ ነገር።
ሜታሎይድአንዳንድ ጊዜ እንደ ብረት አንዳንዴም እንደ ብረት ያልሆነ ምላሽ የሚሰጥ አካል።
ብረት ያልሆነከሌሎች ንጥረ ነገሮች ጋር በኬሚካላዊ ግብረመልሶች ውስጥ ኤሌክትሮኖችን ለማግኘት የሚፈልግ ንጥረ ነገር።
የኬሚካል ንጥረ ነገሮች ወቅታዊ ስርዓት: የኬሚካል ንጥረ ነገሮችን በአቶሚክ ቁጥራቸው መሰረት የመከፋፈል ስርዓት.
ሰው ሠራሽ አካልበቤተ ሙከራ ውስጥ ሰው ሰራሽ በሆነ መንገድ የተገኘ እና ብዙውን ጊዜ በተፈጥሮ ውስጥ የማይከሰት ነው።

ተፈጥሯዊ እና ሰው ሠራሽ አካላት
ዘጠና ሁለት ኬሚካላዊ ንጥረ ነገሮች በምድር ላይ በተፈጥሮ ይከሰታሉ። ቀሪዎቹ በአርቴፊሻል መንገድ በቤተ ሙከራዎች ተገኝተዋል። ሰው ሰራሽ ኬሚካላዊ ንጥረ ነገር በተለምዶ ቅንጣት አፋጣኝ (የሱባቶሚክ ቅንጣቶችን ፍጥነት ለመጨመር የሚያገለግሉ እንደ ኤሌክትሮኖች እና ፕሮቶኖች ያሉ) ወይም የኑክሌር ሬአክተሮች (በኑክሌር ምላሾች ውስጥ የሚወጣውን ሃይል ለመቆጣጠር የሚያገለግሉ መሳሪያዎች) የኑክሌር ምላሾች ውጤት ነው። የመጀመሪያው የተቀናጀ ንጥረ ነገር በአቶሚክ ቁጥር 43 በ 1937 በጣሊያን የፊዚክስ ሊቃውንት C. Perrier እና E. Segre የተገኘው ቴክኒቲየም ነው። ከቴክኒቲየም እና ፕሮሜቲየም በተጨማሪ ሁሉም ሰው ሠራሽ ንጥረ ነገሮች ከዩራኒየም የበለጠ ኒውክሊየሮች አሏቸው። የመጨረሻው ሰው ሰራሽ አካል ሊተርሞሪየም (116) ነው ፣ እና ከዚያ በፊት flerovium (114) ነው።

ሁለት ደርዘን የተለመዱ እና አስፈላጊ ንጥረ ነገሮች
| ስም | ምልክት | የሁሉም አቶሞች መቶኛ * | የኬሚካል ንጥረ ነገሮች ባህሪያት (በተለመደው ክፍል ውስጥ) |
|||
| በአጽናፈ ሰማይ ውስጥ | በምድር ቅርፊት ውስጥ | በባህር ውሃ ውስጥ | በሰው አካል ውስጥ |
|||
| አሉሚኒየም | አል | - | 6,3 | - | - | ቀላል ክብደት, የብር ብረት |
| ካልሲየም | ካ | - | 2,1 | - | 0,02 | በተፈጥሮ ማዕድናት, ዛጎሎች, አጥንቶች ውስጥ ተካትቷል |
| ካርቦን | ከ | - | - | - | 10,7 | የሁሉም ሕያዋን ፍጥረታት መሠረት |
| ክሎሪን | Cl | - | - | 0,3 | - | መርዛማ ጋዝ |
| መዳብ | ኩ | - | - | - | - | ቀይ ብረት ብቻ |
| ወርቅ | አው | - | - | - | - | ቢጫ ብረት ብቻ |
| ሄሊየም | እሱ | 7,1 | - | - | - | በጣም ቀላል ጋዝ |
| ሃይድሮጅን | ኤች | 92,8 | 2,9 | 66,2 | 60,6 | ከሁሉም ንጥረ ነገሮች በጣም ቀላል; ጋዝ |
| አዮዲን | አይ | - | - | - | - | ብረት ያልሆነ; እንደ አንቲሴፕቲክ ጥቅም ላይ ይውላል |
| ብረት | ፌ | - | 2,1 | - | - | መግነጢሳዊ ብረት; ብረት እና ብረት ለማምረት ያገለግላል |
| መራ | ፒ.ቢ | - | - | - | - | ለስላሳ, ከባድ ብረት |
| ማግኒዥየም | ሚ.ግ | - | 2,0 | - | - | በጣም ቀላል ብረት |
| ሜርኩሪ | hg | - | - | - | - | ፈሳሽ ብረት; ከሁለት ፈሳሽ ንጥረ ነገሮች አንዱ |
| ኒኬል | ናይ | - | - | - | - | ዝገት የሚቋቋም ብረት; በሳንቲሞች ውስጥ ጥቅም ላይ ይውላል |
| ናይትሮጅን | ኤን | - | - | - | 2,4 | ጋዝ, የአየር ዋና አካል |
| ኦክስጅን | ስለ | - | 60,1 | 33,1 | 25,7 | ጋዝ, ሁለተኛው አስፈላጊ የአየር ክፍል |
| ፎስፈረስ | አር | - | - | - | 0,1 | ብረት ያልሆነ; ለተክሎች አስፈላጊ |
| ፖታስየም | ለ | - | 1.1 | - | - | ብረት; ለተክሎች አስፈላጊ; በተለምዶ "ፖታሽ" በመባል ይታወቃል. |
* እሴቱ ካልተገለጸ, ንጥረ ነገሩ ከ 0.1 በመቶ ያነሰ ነው.
የቁስ መፈጠር ዋና ምክንያት ትልቅ ባንግ
በአጽናፈ ሰማይ ውስጥ የመጀመሪያው የትኛው ኬሚካላዊ አካል ነው? የሳይንስ ሊቃውንት የዚህ ጥያቄ መልስ በከዋክብት እና በከዋክብት የተፈጠሩ ሂደቶች ላይ ነው ብለው ያምናሉ. አጽናፈ ሰማይ የተፈጠረው ከ12 እስከ 15 ቢሊዮን ዓመታት በፊት በሆነ ጊዜ ውስጥ እንደሆነ ይታመናል። እስከዚህ ቅጽበት ድረስ ከጉልበት በስተቀር ያለ ምንም ነገር አልተፀነሰም። ነገር ግን ይህን ሃይል ወደ ከፍተኛ ፍንዳታ (ቢግ ባንግ እየተባለ የሚጠራው) የሆነ ነገር ተፈጠረ። ከቢግ ባንግ በኋላ ባሉት ሰከንዶች ውስጥ ቁስ አካል መፈጠር ጀመረ።
የመጀመሪያዎቹ ቀላል የቁስ ዓይነቶች ፕሮቶን እና ኤሌክትሮኖች ነበሩ። አንዳንዶቹ ወደ ሃይድሮጂን አተሞች ይጣመራሉ. የኋለኛው አንድ ፕሮቶን እና አንድ ኤሌክትሮን ያካትታል; ሊኖር የሚችለው ቀላሉ አቶም ነው።

ቀስ በቀስ፣ በረጅም ጊዜ ውስጥ፣ የሃይድሮጂን አተሞች በተወሰኑ የጠፈር ክልሎች ውስጥ አንድ ላይ መሰብሰብ ጀመሩ፣ ጥቅጥቅ ያሉ ደመናዎችን ፈጠሩ። በእነዚህ ደመናዎች ውስጥ ያለው ሃይድሮጅን በስበት ኃይል ወደ ጥቅጥቅ ያሉ ቅርጾች ተወስዷል. በመጨረሻም እነዚህ የሃይድሮጂን ደመናዎች ጥቅጥቅ ያሉ ሆኑ ከዋክብትን መፍጠር ቻሉ።
ከዋክብት እንደ አዲስ ንጥረ ነገሮች ኬሚካላዊ ሪአክተሮች
ኮከብ በቀላሉ የኑክሌር ምላሾችን ኃይል የሚያመነጭ የቁስ አካል ነው። ከእነዚህ ግብረመልሶች ውስጥ በጣም የተለመደው የአራት ሃይድሮጂን አተሞች ጥምረት አንድ ሄሊየም አቶም መፍጠር ነው። ከዋክብት መፈጠር እንደጀመሩ ሂሊየም በአጽናፈ ሰማይ ውስጥ የሚታየው ሁለተኛው ንጥረ ነገር ሆነ።
ከዋክብት እያደጉ ሲሄዱ ከሃይድሮጂን-ሄሊየም ኑክሌር ምላሽ ወደ ሌሎች ዓይነቶች ይለወጣሉ. በውስጣቸው, የሂሊየም አተሞች የካርቦን አተሞች ይፈጥራሉ. በኋላ የካርቦን አተሞች ኦክስጅን, ኒዮን, ሶዲየም እና ማግኒዥየም ይፈጥራሉ. አሁንም በኋላ, ኒዮን እና ኦክስጅን እርስ በርስ በመዋሃድ ማግኒዚየም ይፈጥራሉ. እነዚህ ምላሾች በሚቀጥሉበት ጊዜ, ብዙ እና ተጨማሪ የኬሚካል ንጥረ ነገሮች ይፈጠራሉ.
የኬሚካል ንጥረ ነገሮች የመጀመሪያ ስርዓቶች
ከ 200 ዓመታት በፊት, ኬሚስቶች እነሱን ለመመደብ መንገዶች መፈለግ ጀመሩ. በአስራ ዘጠነኛው ክፍለ ዘመን አጋማሽ ላይ ወደ 50 የሚጠጉ የኬሚካል ንጥረ ነገሮች ይታወቃሉ. ኬሚስቶች ለመፍታት ከሚፈልጉት ጥያቄዎች ውስጥ አንዱ። በሚከተለው መልኩ የተቀቀለ፡ የኬሚካል ንጥረ ነገር ንጥረ ነገር ከማንኛውም ንጥረ ነገር ፈጽሞ የተለየ ነው? ወይስ አንዳንድ ንጥረ ነገሮች በሆነ መንገድ ከሌሎች ጋር ይዛመዳሉ? አንድ የሚያደርጋቸው የጋራ ህግ አለ?
ኬሚስቶች የተለያዩ የኬሚካላዊ ንጥረ ነገሮችን ስርዓቶች አቅርበዋል. ስለዚህ ለምሳሌ እንግሊዛዊው ኬሚስት ዊልያም ፕሮውት እ.ኤ.አ. በዚያን ጊዜ የበርካታ ንጥረ ነገሮች የአቶሚክ ስብስቦች ከሃይድሮጂን ብዛት ጋር በተያያዘ በጄ.ዳልተን ተቆጥረዋል። ነገር ግን፣ ይህ ለካርቦን፣ ናይትሮጅን፣ ኦክሲጅን በግምት ከሆነ፣ 35.5 ክብደት ያለው ክሎሪን በዚህ እቅድ ውስጥ አልገባም።
ጀርመናዊው ኬሚስት ጆሃን ቮልፍጋንግ ዶቤሬይነር (1780-1849) በ1829 እንዳሳየው ሃሎጅን ቡድን ከሚባሉት ሶስት አካላት (ክሎሪን፣ ብሮሚን እና አዮዲን) እንደ አንጻራዊ የአቶሚክ ብዛት ሊከፋፈሉ ይችላሉ። የአቶሚክ ክብደት ብሮሚን (79.9) የክሎሪን (35.5) እና አዮዲን (127) ማለትም 35.5 + 127 ÷ 2 = 81.25 (ወደ 79.9 የሚጠጋ) የአቶሚክ ክብደት አማካኝ ማለት ይቻላል ማለት ይቻላል። ይህ ከኬሚካላዊ ንጥረ ነገሮች ቡድን ውስጥ አንዱን ለመገንባት የመጀመሪያው አቀራረብ ነበር. ዶበሪነር ሁለት ተጨማሪ የሶስትዮሽ አካላትን አግኝቷል, ነገር ግን አጠቃላይ ወቅታዊ ህግን ማዘጋጀት አልቻለም.
የኬሚካል ንጥረ ነገሮች ወቅታዊ ሰንጠረዥ እንዴት ታየ?
አብዛኛዎቹ ቀደምት የምደባ መርሃግብሮች በጣም ስኬታማ አልነበሩም። ከዚያም፣ በ1869 አካባቢ፣ ከሞላ ጎደል ተመሳሳይ ግኝት በሁለት ኬሚስቶች በአንድ ጊዜ ተደረገ። ሩሲያዊው ኬሚስት ዲሚትሪ ሜንዴሌቭ (1834-1907) እና ጀርመናዊው ኬሚስት ጁሊየስ ሎታር ሜየር (1830-1895) ተመሳሳይ አካላዊ እና ኬሚካላዊ ባህሪያት ያላቸውን አካላት በታዘዘ የቡድኖች፣ ተከታታይ እና ወቅቶች የማደራጀት ሀሳብ አቅርበዋል። በዚሁ ጊዜ ሜንዴሌቭ እና ሜየር የኬሚካል ንጥረነገሮች ባህሪያት በአቶሚክ ክብደታቸው ላይ በመመርኮዝ በየጊዜው እንደሚደጋገሙ ጠቁመዋል.
ዛሬ ሜንዴሌቭ ሜየር ያላደረገውን አንድ እርምጃ በመውሰዱ በአጠቃላይ የወቅቱ ህግ ፈላጊ ነው ተብሎ ይታሰባል። ሁሉም ንጥረ ነገሮች በጊዜ ሰንጠረዥ ውስጥ ሲቀመጡ, በውስጡ አንዳንድ ክፍተቶች ታዩ. ሜንዴሌቭ እነዚህ ገና ያልተገኙ ንጥረ ነገሮች የሚገኙባቸው ቦታዎች እንደሆኑ ተንብዮ ነበር።
ሆኖም እሱ የበለጠ ሄደ። ሜንዴሌቭ የእነዚህን ገና ያልተገኙ ንጥረ ነገሮች ባህሪያት ተንብዮአል። በየወቅቱ ጠረጴዛው ላይ የት እንደሚገኙ ስለሚያውቅ ንብረታቸውን ሊተነብይ ይችላል። እያንዳንዱ የተተነበየ ኬሚካላዊ ንጥረ ነገር ሜንዴሌቭ ፣ የወደፊቱ ጋሊየም ፣ ስካንዲየም እና ጀርማኒየም የወቅቱን ህግ ካተመ አስር ዓመት ባልሞላ ጊዜ ውስጥ መገኘቱ ትኩረት የሚስብ ነው።
ወቅታዊ ሰንጠረዥ አጭር ቅጽ
በተለያዩ ሳይንቲስቶች የወቅቱ ስርዓት ግራፊክ ውክልና ምን ያህል ልዩነቶች እንደቀረቡ ለማስላት ሙከራዎች ነበሩ። ከ 500 በላይ ሆኖ ተገኝቷል. ከዚህም በላይ 80% ከጠቅላላው የአማራጮች ቁጥር ሰንጠረዦች ናቸው, የተቀሩት ደግሞ የጂኦሜትሪክ ቅርጾች, የሒሳብ ኩርባዎች, ወዘተ ናቸው. - ረጅም, ረጅም እና መሰላል (ፒራሚዳል). የኋለኛው ሐሳብ የቀረበው በታላቁ የፊዚክስ ሊቅ N. Bohr.
ከታች ያለው ምስል አጭር ቅጹን ያሳያል.

በውስጡም የኬሚካል ንጥረነገሮች በአቶሚክ ቁጥራቸው ከግራ ወደ ቀኝ እና ከላይ ወደ ታች በቅደም ተከተል ተቀምጠዋል. ስለዚህ የፔርዲክቲክ ሠንጠረዥ የመጀመሪያው ኬሚካላዊ ንጥረ ነገር ሃይድሮጂን አቶሚክ ቁጥር 1 አለው ምክንያቱም የሃይድሮጂን አተሞች አስኳል አንድ እና አንድ ፕሮቶን ብቻ ይይዛሉ። በተመሳሳይም የኦክስጂን አተሞች ኒውክሊየሮች 8 ፕሮቶኖች ስላሏቸው ኦክስጅን 8 አቶሚክ ቁጥር አለው (ከዚህ በታች ያለውን ምስል ይመልከቱ)።

የወቅቱ ስርዓት ዋና መዋቅራዊ ቁርጥራጮች ወቅቶች እና የንጥረ ነገሮች ቡድን ናቸው። በስድስት ጊዜ ውስጥ ሁሉም ሴሎች ይሞላሉ, ሰባተኛው ገና አልተጠናቀቀም (አካላት 113, 115, 117 እና 118, በቤተ ሙከራ ውስጥ የተዋሃዱ ቢሆንም, እስካሁን በይፋ አልተመዘገቡም እና ስሞች የላቸውም).
ቡድኖች በዋና (A) እና ሁለተኛ (ለ) ንዑስ ቡድኖች ይከፈላሉ. እያንዳንዳቸው አንድ ተከታታይ መስመርን የያዙ የመጀመሪያዎቹ ሶስት ወቅቶች ንጥረ ነገሮች በ A-ንዑስ ቡድኖች ውስጥ ብቻ ተካትተዋል። የተቀሩት አራት ወቅቶች እያንዳንዳቸው ሁለት ረድፎችን ያካትታሉ.
በተመሳሳዩ ቡድን ውስጥ ያሉ የኬሚካል ንጥረነገሮች ተመሳሳይ የኬሚካል ባህሪያት አላቸው. ስለዚህ, የመጀመሪያው ቡድን የአልካላይን ብረቶች, ሁለተኛው - የአልካላይን ምድር ያካትታል. በተመሳሳይ ጊዜ ውስጥ ያሉ ንጥረ ነገሮች ከአልካላይን ብረት ወደ ክቡር ጋዝ የሚቀይሩ ባህሪያት አሏቸው. ከታች ያለው ምስል ከንብረቶቹ አንዱ - አቶሚክ ራዲየስ - በሰንጠረዡ ውስጥ ለግለሰብ አካላት እንዴት እንደሚለወጥ ያሳያል.
የፔርዲክቲክ ሰንጠረዥ የረጅም ጊዜ ቅጽ
ከታች ባለው ስእል ይታያል እና በሁለት አቅጣጫዎች, በመደዳ እና በአምዶች የተከፈለ ነው. እንደ አጭር ቅፅ ሰባት ጊዜ ረድፎች እና 18 አምዶች ቡድኖች ወይም ቤተሰቦች ይባላሉ። እንደ እውነቱ ከሆነ የቡድኖች ቁጥር ከ 8 በአጭር ጊዜ ወደ 18 በረጅም ጊዜ መጨመር የተገኘው ሁሉንም ንጥረ ነገሮች ከ 4 ኛ ጀምሮ ባሉት ጊዜያት በሁለት ሳይሆን በአንድ መስመር ውስጥ በማስቀመጥ ነው.
በሠንጠረዡ አናት ላይ እንደሚታየው ሁለት የተለያዩ የቁጥር ስርዓቶች ለቡድኖች ጥቅም ላይ ይውላሉ. የሮማውያን ቁጥር ሥርዓት (IA, IIA, IIB, IVB, ወዘተ.) በተለምዶ በአሜሪካ ውስጥ ታዋቂ ነበር. ሌላ ስርዓት (1, 2, 3, 4, ወዘተ) በአውሮፓ ውስጥ በተለምዶ ጥቅም ላይ ይውላል, እና ከጥቂት አመታት በፊት በአሜሪካ ውስጥ ጥቅም ላይ እንዲውል ይመከራል.

ከላይ ባሉት ሥዕላዊ መግለጫዎች ላይ የወቅቱ የጠረጴዛዎች ገጽታ ትንሽ አሳሳች ነው ፣ እንደማንኛውም የታተመ ሠንጠረዥ። ይህ የሆነበት ምክንያት በጠረጴዛዎቹ ግርጌ ላይ የሚታዩት ሁለቱ የንጥረ ነገሮች ቡድን በትክክል በውስጣቸው መቀመጥ አለባቸው. ላንታኒድስ፣ ለምሳሌ፣ በባሪየም (56) እና በ hafnium (72) መካከል ያለው የጊዜ 6 ነው። በተጨማሪም አክቲኒዶች በራዲየም (88) እና ሩዘርፎርዲየም (104) መካከል ያለው የጊዜ 7 ናቸው። በጠረጴዛ ላይ ከተለጠፉ, በወረቀት ወይም በግድግዳ ሠንጠረዥ ላይ ለመገጣጠም በጣም ሰፊ ይሆናል. ስለዚህ, እነዚህን ንጥረ ነገሮች በጠረጴዛው ግርጌ ላይ ማስቀመጥ የተለመደ ነው.
ወቅታዊው ሰንጠረዥ ለመረዳት የሚያስቸግር መስሎ ከታየ እርስዎ ብቻዎን አይደሉም! ምንም እንኳን የእሱን መርሆዎች ለመረዳት አስቸጋሪ ሊሆን ቢችልም, ከእሱ ጋር አብሮ ለመስራት መማር በተፈጥሮ ሳይንስ ጥናት ውስጥ ይረዳል. ለመጀመር የሠንጠረዡን መዋቅር እና ስለ እያንዳንዱ የኬሚካል ንጥረ ነገር ምን መረጃ ከእሱ መማር እንደሚቻል ማጥናት. ከዚያ የእያንዳንዱን ንጥረ ነገር ባህሪያት ማሰስ መጀመር ይችላሉ. እና በመጨረሻም ፣ ወቅታዊውን ሰንጠረዥ በመጠቀም ፣ በአንድ የተወሰነ የኬሚካል ንጥረ ነገር አቶም ውስጥ የኒውትሮን ብዛት መወሰን ይችላሉ።
እርምጃዎች
ክፍል 1
የጠረጴዛ መዋቅር- ለምሳሌ የሠንጠረዡ የመጀመሪያ ረድፍ አቶሚክ ቁጥር 1 ያለው ሃይድሮጂን እና አቶሚክ ቁጥር 2 ያለው ሂሊየም ይዟል.ነገር ግን እነሱ በተለያየ ቡድን ውስጥ በመሆናቸው በተቃራኒ ጫፎች ላይ ይገኛሉ.
-
ተመሳሳይ አካላዊ እና ኬሚካዊ ባህሪያት ያላቸውን ንጥረ ነገሮች ስለሚያካትቱ ቡድኖች ይወቁ።የእያንዳንዱ ቡድን አካላት በተዛማጅ ቋሚ አምድ ውስጥ ይገኛሉ. እንደ አንድ ደንብ, በተመሳሳይ ቀለም ይጠቁማሉ, ይህም ተመሳሳይ አካላዊ እና ኬሚካዊ ባህሪያት ያላቸውን ንጥረ ነገሮች ለመለየት እና ባህሪያቸውን ለመተንበይ ይረዳል. የአንድ የተወሰነ ቡድን ሁሉም ንጥረ ነገሮች በውጫዊው ሽፋን ውስጥ ተመሳሳይ ኤሌክትሮኖች ቁጥር አላቸው.
- ሃይድሮጅን ለሁለቱም የአልካላይን ብረቶች ቡድን እና ለ halogens ቡድን ሊሰጥ ይችላል. በአንዳንድ ሠንጠረዦች በሁለቱም ቡድኖች ውስጥ ይገለጻል.
- በአብዛኛዎቹ ሁኔታዎች ቡድኖቹ ከ 1 እስከ 18 ተቆጥረዋል, እና ቁጥሮቹ በጠረጴዛው የላይኛው ወይም የታችኛው ክፍል ላይ ይቀመጣሉ. ቁጥሮች በሮማንኛ (ለምሳሌ IA) ወይም በአረብኛ (ለምሳሌ 1A ወይም 1) ቁጥሮች ሊሰጡ ይችላሉ።
- በአምዱ ላይ ከላይ ወደ ታች ሲንቀሳቀሱ "ቡድኑን እያሰሱ ነው" ይላሉ.
-
በሠንጠረዡ ውስጥ ባዶ ሴሎች ለምን እንዳሉ ይወቁ.ንጥረ ነገሮች በአቶሚክ ቁጥራቸው ብቻ ሳይሆን በቡድኖች (የአንድ ቡድን አካላት ተመሳሳይ አካላዊ እና ኬሚካላዊ ባህሪያት አላቸው) የታዘዙ ናቸው. ይህ የአንድ አካል ባህሪ እንዴት እንደሆነ ለመረዳት ቀላል ያደርገዋል። ነገር ግን የአቶሚክ ቁጥሩ እየጨመረ ሲሄድ ወደ ተጓዳኝ ቡድን ውስጥ የሚወድቁ ንጥረ ነገሮች ሁልጊዜ አይገኙም, ስለዚህ በጠረጴዛው ውስጥ ባዶ ሴሎች አሉ.
- ለምሳሌ, የመጀመሪያዎቹ 3 ረድፎች ባዶ ሴሎች አሏቸው, ምክንያቱም የሽግግር ብረቶች የሚገኙት ከአቶሚክ ቁጥር 21 ብቻ ነው.
- ከ 57 እስከ 102 ያሉት የአቶሚክ ቁጥሮች ያላቸው ንጥረ ነገሮች ያልተለመዱ የምድር ንጥረ ነገሮች ናቸው ፣ እና እነሱ ብዙውን ጊዜ በጠረጴዛው ታችኛው ቀኝ ጥግ ላይ በተለየ ንዑስ ቡድን ውስጥ ይቀመጣሉ።
-
የሠንጠረዡ እያንዳንዱ ረድፍ ክፍለ ጊዜን ይወክላል.በተመሳሳይ ጊዜ ውስጥ ያሉ ሁሉም ንጥረ ነገሮች ኤሌክትሮኖች በአተሞች ውስጥ የሚገኙበት የአቶሚክ ምህዋሮች ተመሳሳይ ቁጥር አላቸው. የምሕዋር ብዛት ከወቅቱ ቁጥር ጋር ይዛመዳል። ሠንጠረዡ 7 ረድፎችን ማለትም 7 ጊዜዎችን ይዟል.
- ለምሳሌ የመጀመርያው ክፍለ ጊዜ ንጥረ ነገሮች አተሞች አንድ ምህዋር አላቸው ፣ እና የሰባተኛው ክፍለ ጊዜ ንጥረ ነገሮች አተሞች 7 ምህዋር አላቸው።
- እንደ አንድ ደንብ, ክፍለ-ጊዜዎች በሠንጠረዡ በግራ በኩል ከ 1 እስከ 7 ባሉት ቁጥሮች ይገለጣሉ.
- ከግራ ወደ ቀኝ መስመር ስትሄድ "ፔርደር እያለህ እየቃኘህ ነው" ይባላል።
-
በብረታ ብረት, በሜታሎይድ እና በብረት ያልሆኑ መካከል ያለውን ልዩነት ይማሩ.የንብረቱ አይነት ምን እንደሆነ መወሰን ከቻሉ የአንድን ንጥረ ነገር ባህሪያት በተሻለ ሁኔታ ይረዱዎታል. ለመመቻቸት, በአብዛኛዎቹ ጠረጴዛዎች ውስጥ, ብረቶች, ሜታሎይድ እና ብረት ያልሆኑ በተለያየ ቀለም ይጠቁማሉ. ብረቶች በግራ በኩል ናቸው, እና ብረቶች ያልሆኑ በጠረጴዛው በቀኝ በኩል ናቸው. Metalloids በመካከላቸው ይገኛሉ.
ክፍል 2
የንጥል ስያሜዎች-
እያንዳንዱ ንጥረ ነገር በአንድ ወይም በሁለት የላቲን ፊደላት ይሰየማል.እንደ አንድ ደንብ, የኤለመንቱ ምልክት በተዛመደው ሕዋስ መሃል ላይ በትልልቅ ፊደላት ይታያል. ምልክት በአብዛኛዎቹ ቋንቋዎች አንድ አይነት አካል የሆነ አህጽሮተ ቃል ነው። ሙከራዎችን ሲያደርጉ እና ከኬሚካላዊ እኩልታዎች ጋር ሲሰሩ የንጥሎቹ ምልክቶች በብዛት ጥቅም ላይ ይውላሉ, ስለዚህ እነሱን ማስታወስ ጠቃሚ ነው.
- በተለምዶ የኤለመንቱ ምልክቶች ለላቲን ስማቸው አጠር ያሉ ናቸው፣ ምንም እንኳን ለአንዳንዶች በተለይም በቅርብ ጊዜ የተገኙ ንጥረ ነገሮች ከተለመዱት ስም የተወሰዱ ናቸው። ለምሳሌ፣ ሄሊየም የሚለው ምልክት በአብዛኛዎቹ ቋንቋዎች ለሚታወቀው ስም ቅርብ በሆነው ሄ በሚለው ምልክት ነው። በተመሳሳይ ጊዜ ብረት ፌ ተብሎ የተሰየመ ሲሆን ይህም የላቲን ስሙ ምህጻረ ቃል ነው.
-
በሠንጠረዡ ውስጥ ከተሰጠ ለኤለመንቱ ሙሉ ስም ትኩረት ይስጡ.ይህ የንጥሉ "ስም" በመደበኛ ጽሑፎች ውስጥ ጥቅም ላይ ይውላል. ለምሳሌ "ሄሊየም" እና "ካርቦን" የንጥረ ነገሮች ስሞች ናቸው. ብዙውን ጊዜ, ሁልጊዜ ባይሆንም, የንጥረ ነገሮች ሙሉ ስሞች በኬሚካላዊ ምልክታቸው ስር ይሰጣሉ.
- አንዳንድ ጊዜ የንጥሎቹ ስሞች በሰንጠረዡ ውስጥ አልተገለጹም እና የኬሚካዊ ምልክቶቻቸው ብቻ ተሰጥተዋል.
-
የአቶሚክ ቁጥር ያግኙ።ብዙውን ጊዜ የአንድ ንጥረ ነገር አቶሚክ ቁጥር በተዛማጅ ሕዋስ አናት ላይ, በመሃል ወይም በማእዘኑ ላይ ይገኛል. እንዲሁም ከምልክቱ ወይም ከኤለመንት ስም በታች ሊታይ ይችላል። ንጥረ ነገሮች አቶሚክ ቁጥሮች ከ1 እስከ 118 አላቸው።
- የአቶሚክ ቁጥሩ ሁልጊዜ ኢንቲጀር ነው።
-
ያስታውሱ የአቶሚክ ቁጥሩ በአንድ አቶም ውስጥ ካሉት ፕሮቶኖች ብዛት ጋር እንደሚዛመድ።ሁሉም የአንድ ንጥረ ነገር አተሞች አንድ አይነት ፕሮቶን ይይዛሉ። ከኤሌክትሮኖች በተለየ፣ በአንድ ንጥረ ነገር አተሞች ውስጥ ያሉት የፕሮቶኖች ብዛት ቋሚ ሆኖ ይቆያል። ያለበለዚያ ሌላ የኬሚካል ንጥረ ነገር ይወጣ ነበር!
-
ወቅታዊው ሰንጠረዥ ወይም ወቅታዊ የኬሚካል ንጥረ ነገሮች ሰንጠረዥ ከላይ በግራ በኩል ይጀምራል እና በመጨረሻው የጠረጴዛው መስመር መጨረሻ (ከታች በስተቀኝ) ያበቃል. በሰንጠረዡ ውስጥ ያሉት ንጥረ ነገሮች በአቶሚክ ቁጥራቸው ከፍ ወዳለ ቅደም ተከተል ከግራ ወደ ቀኝ ተደርድረዋል። የአቶሚክ ቁጥሩ በአንድ አቶም ውስጥ ስንት ፕሮቶኖች እንዳሉ ይነግርዎታል። በተጨማሪም የአቶሚክ ቁጥሩ እየጨመረ ሲሄድ የአቶሚክ ብዛት ይጨምራል. ስለዚህ በፔርዲክቲክ ሠንጠረዥ ውስጥ ያለው ንጥረ ነገር በሚገኝበት ቦታ የአቶሚክ መጠኑን መወሰን ይችላሉ።
እንደሚመለከቱት ፣ እያንዳንዱ ቀጣይ ንጥረ ነገር ከእሱ በፊት ካለው ንጥረ ነገር አንድ ተጨማሪ ፕሮቶን ይይዛል።የአቶሚክ ቁጥሮችን ሲመለከቱ ይህ ግልጽ ነው። ከግራ ወደ ቀኝ ሲንቀሳቀሱ የአቶሚክ ቁጥሮች በአንድ ይጨምራሉ። ንጥረ ነገሮቹ በቡድን ስለሚደራጁ አንዳንድ የሰንጠረዥ ሴሎች ባዶ ሆነው ይቆያሉ።
የሜንዴሌቭ ወቅታዊ ጠረጴዛ
የሜንዴሌቭን ወቅታዊ የኬሚካል ንጥረ ነገሮች ሠንጠረዥ መገንባት ከቁጥር ፅንሰ-ሀሳብ እና ከሥነ-ሥርዓተ-ጥበባት ባህሪያት ጊዜ ጋር ይዛመዳል. የሃዳማርድ ማትሪክስ በተመጣጣኝ እና ያልተለመዱ ትዕዛዞች ማትሪክስ የጎጆ ማትሪክስ አካላት መዋቅራዊ መሰረት ይፈጥራል፡የመጀመሪያው (ኦዲን)፣ ሁለተኛ (ኡለር)፣ ሶስተኛ (መርሴን)፣ አራተኛ (ሃዳማርድ) እና አምስተኛ (ፌርማት) ትዕዛዞች።
ያንን የክብደት መጠን 4 ለማየት ቀላል ነው። ክሃዳማርድ ማትሪክስ ከአቶሚክ ክብደት ጋር ከማይነቃነቅ ንጥረ ነገሮች ጋር ይዛመዳል ይህም አራት ብዜት ነው፡- ሂሊየም 4፣ ኒዮን 20፣ አርጎን 40 (39.948)፣ ወዘተ. ጀርመን 72.
ከመርሴኔ ማትሪክስ ትዕዛዝ 4 ጋር ይመስላል ክ-1, በተቃራኒው, ሁሉም ነገር ንቁ, መርዛማ, አጥፊ እና የሚበላሽ ነው. ነገር ግን እነዚህ ራዲዮአክቲቭ ንጥረ ነገሮች ናቸው - የኃይል ምንጮች, እና እርሳስ 207 (የመጨረሻው ምርት, መርዛማ ጨዎችን). ፍሎራይን በእርግጥ 19 ነው. የመርሴን ማትሪክስ ትዕዛዞች አክቲኒየም ተከታታይ ከሚባሉት ራዲዮአክቲቭ ንጥረ ነገሮች ቅደም ተከተል ጋር ይዛመዳሉ: ዩራኒየም 235, ፕሉቶኒየም 239 (ከዩራኒየም የበለጠ ኃይለኛ የአቶሚክ ሃይል ምንጭ የሆነ isotope), ወዘተ. እነዚህም አልካሊ ብረቶች ሊቲየም 7፣ ሶዲየም 23 እና ፖታሺየም 39 ናቸው።

ጋሊየም - አቶሚክ ክብደት 68
ትዕዛዞች 4 ክ-2 የዩለር ማትሪክስ (ድርብ መርሴኔ) ከናይትሮጅን 14 (የከባቢ አየር መሠረት) ጋር ይዛመዳል። የጠረጴዛ ጨው በሁለት “መርሴን መሰል” አተሞች የሶዲየም 23 እና ክሎሪን 35 አተሞች ይመሰረታል፣ ይህ ጥምረት ለኡለር ማትሪክስ ብቻ የተለመደ ነው። የ 35.4 ክብደት ያለው ተጨማሪ ግዙፍ ክሎሪን ከሃዳማርድ ልኬት ትንሽ አጭር ነው 36. የተለመዱ የጨው ክሪስታሎች: ኩብ (ማለትም, የዋህ ገጸ ባህሪ, ሃዳማርስ) እና ኦክታቴሮን (ይበልጥ ፈታኝ ነው, ይህ ምንም ጥርጥር የለውም Euler).
በአቶሚክ ፊዚክስ ፣ ብረት 56 - ኒኬል 59 ሽግግር ትልቅ አስኳል (ሃይድሮጂን ቦምብ) እና መበስበስ (የዩራኒየም ቦምብ) ውህደት በሚፈጠርበት ጊዜ ኃይል በሚሰጡ ንጥረ ነገሮች መካከል ያለው ድንበር ነው። ትዕዛዙ 58 ዝነኛ ነው ምክንያቱም ለእሱ በሀዳማርድ ማትሪክስ አናሎግ ብቻ ሳይሆን በዲያግናል ላይ ዜሮዎች ያሉት የቤሌቪች ማትሪክስ ፣ እንዲሁም ለእሱ ብዙ ክብደት ያላቸው ማትሪክስ ስለሌለ - የቅርቡ orthogonal W (58,53) በእያንዳንዱ አምድ እና ረድፍ 5 ዜሮዎች አሉት (ጥልቅ ክፍተት).
ከ Fermat ማትሪክስ እና የትዕዛዝ መተኪያዎቻቸው ጋር በተዛመደ ተከታታይ ውስጥ ክ+1፣ በእጣ ፈንታ 257 ፌርሚ ያስከፍላል። ምንም ማለት አይችሉም፣ ትክክለኛ ምት። እዚህ ወርቅ ነው 197. መዳብ 64 (63.547) እና ብር 108 (107.868), የኤሌክትሮኒክስ ምልክቶች, ይመስላል ወርቅ አይደርሱም እና ይበልጥ መጠነኛ ሃዳማርድ ማትሪክስ ጋር ይዛመዳሉ. መዳብ, የአቶሚክ ክብደቱ ከ 63 ብዙም ያልራቀ, በኬሚካል ንቁ - አረንጓዴ ኦክሳይዶች በደንብ ይታወቃሉ.
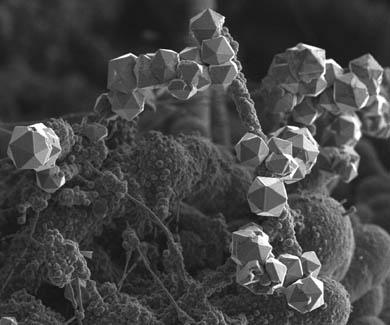
በከፍተኛ ማጉላት ስር ያሉ የቦር ክሪስታሎች
ከ ወርቃማ ጥምርታቦሮን ተያይዟል - ከሌሎች ንጥረ ነገሮች መካከል ያለው የአቶሚክ ብዛት ወደ 10 ቅርብ ነው (በይበልጥ በትክክል 10.8 ፣ የአቶሚክ ክብደት ለልዩ ቁጥሮች ቅርበት እንዲሁ ይጎዳል)። ቦሮን በጣም የተወሳሰበ አካል ነው። ቦህር በራሱ የሕይወት ታሪክ ውስጥ ግራ የሚያጋባ ሚና ይጫወታል። በእሱ መዋቅሮች ውስጥ ያለው የማዕቀፍ መዋቅር ከአልማዝ የበለጠ የተወሳሰበ ነው. ምንም እንኳን ብዙ ሳይንቲስቶች ከዚህ ጋር በተያያዙ ጥናቶች የኖቤል ሽልማቶችን ቢያገኙም ቦሮን ማንኛውንም ቆሻሻ እንዲወስድ የሚፈቅድ ልዩ የኬሚካል ትስስር በጣም በደንብ አልተረዳም። የቦሮን ክሪስታል ቅርፅ icosahedron ነው, አምስት ትሪያንግሎች አንድ ጫፍ ይመሰርታሉ.
የፕላቲኒየም ምስጢር. አምስተኛው አካል, እንደ ወርቅ ያሉ ክቡር ብረቶች ያለ ጥርጥር ነው. በሃዳማርድ ልኬት 4 ላይ እገዳ ክ, ለ 1 ትልቅ.

የተረጋጋ isotope ዩራኒየም 238
ነገር ግን የፌርማት ቁጥሮች ብርቅ መሆናቸውን አስታውስ (የቅርቡ 257 ነው)። ቤተኛ የወርቅ ክሪስታሎች ወደ ኪዩብ ቅርብ የሆነ ቅርጽ አላቸው፣ ነገር ግን ፔንታግራም እንዲሁ ያበራል። የቅርብ ጎረቤቱ ፕላቲነም ፣ ክቡር ብረት ፣ ከአቶሚክ ክብደት ከ 4 እጥፍ ያነሰ ከወርቅ 197. ፕላቲኒየም የአቶሚክ ክብደት 193 አይደለም ፣ ግን በተወሰነ ደረጃ ጨምሯል ፣ 194 (የዩለር ማትሪክስ ቅደም ተከተል)። ትንሽ ነገር ግን ወደ ጥቂት ተጨማሪ ጠበኛ አካላት ካምፕ ውስጥ ያመጣታል። ማስታወስ ጠቃሚ ነው, ከማይነቃነቅ ጋር (ይሟሟታል, ምናልባትም, በ aqua regia) ውስጥ, ፕላቲኒየም ለኬሚካላዊ ሂደቶች ንቁ ማበረታቻ ሆኖ ያገለግላል.
ስፖንጊ ፕላቲነም በክፍል ሙቀት ውስጥ ሃይድሮጅንን ያቀጣጥላል. የፕላቲኒየም ተፈጥሮ ሰላማዊ አይደለም, ኢሪዲየም 192 በጸጥታ ይሠራል (የ isotopes 191 እና 193 ድብልቅ). እሱ እንደ መዳብ ነው ፣ ግን ከወርቅ ክብደት እና ባህሪ ጋር።
በኒዮን 20 እና በሶዲየም 23 መካከል የአቶሚክ ክብደት 22 የሆነ ንጥረ ነገር የለም።በእርግጥ የአቶሚክ ክብደት ዋና ባህሪ ነው። ነገር ግን isotopes መካከል, በተራው, ደግሞ ቁጥሮች ንብረቶች እና orthogonal ቤዝ ተዛማጅ matrices ጋር ንብረቶች የማወቅ ጉጉ ግንኙነት. እንደ ኑክሌር ነዳጅ, isotope uranium 235 (የመርሴን ማትሪክስ ቅደም ተከተል) ከፍተኛ ጥቅም አለው, በዚህ ውስጥ እራሱን የሚቋቋም የኑክሌር ሰንሰለት ምላሽ ማግኘት ይቻላል. በተፈጥሮ ውስጥ, ይህ ንጥረ ነገር በተረጋጋ ቅርጽ ዩራኒየም 238 (የዩለር ማትሪክስ ቅደም ተከተል) ይከሰታል. 13 የአቶሚክ ክብደት ያለው አካል የለም። ግርግርን በተመለከተ፣የጊዜያዊ ሠንጠረዥ የተረጋጉ ንጥረ ነገሮች ውሱን እና በአስራ ሦስተኛው-ትዕዛዝ ማትሪክስ ላይ በሚታየው እንቅፋት ምክንያት ከፍተኛ-ደረጃ ማትሪክስ ለማግኘት ያለው ችግር ይዛመዳል።
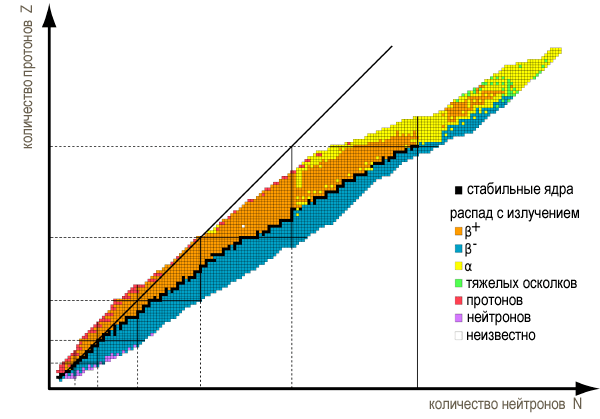
የኬሚካል ንጥረ ነገሮች ኢሶፖፖች, የመረጋጋት ደሴት
ሁሉም የኬሚካል ንጥረነገሮች በአተሞቻቸው መዋቅር ላይ እንዲሁም በዲ.አይ. ወቅታዊ ስርዓት ውስጥ ባለው ቦታ ላይ ተመስርተው ሊታወቁ ይችላሉ. ሜንዴሌቭ. ብዙውን ጊዜ የኬሚካል ንጥረ ነገር ባህሪያት በሚከተለው እቅድ መሰረት ይሰጣሉ.
- የኬሚካል ንጥረ ነገር ምልክት, እንዲሁም ስሙን ያመልክቱ;
- በዲ.አይ. ወቅታዊ ስርዓት ውስጥ ባለው ንጥረ ነገር አቀማመጥ ላይ በመመስረት. ሜንዴሌቭ ኤለመንቱ የሚገኝበትን መደበኛ ፣ የጊዜ ቁጥር እና ቡድን (የንዑስ ቡድን ዓይነት) ያመለክታሉ።
- በአተም መዋቅር ላይ በመመስረት የኑክሌር ክፍያን, የጅምላ ቁጥርን, የኤሌክትሮኖች ብዛት, ፕሮቶን እና ኒውትሮን በአተም ውስጥ;
- የኤሌክትሮኒክ ውቅረትን ይፃፉ እና የቫሌሽን ኤሌክትሮኖችን ያመልክቱ;
- የኤሌክትሮን ግራፊክ ቀመሮችን በመሬት ውስጥ ለቫሌሽን ኤሌክትሮኖች ይሳሉ እና ደስተኛ (ከተቻለ) ግዛቶች;
- የንብረቱን ቤተሰብ, እንዲሁም የእሱን አይነት (ብረት ወይም ብረት ያልሆነ) ያመልክቱ;
- የከፍተኛ ኦክሳይድ እና ሃይድሮክሳይድ ቀመሮችን ከንብረታቸው አጭር መግለጫ ጋር ያመልክቱ።
- የአንድ ኬሚካላዊ ንጥረ ነገር ዝቅተኛ እና ከፍተኛ የኦክሳይድ ሁኔታዎችን ያመልክቱ።
የቫናዲየም (V) ምሳሌን በመጠቀም የኬሚካል ንጥረ ነገር ባህሪያት.
ከላይ በተገለጸው እቅድ መሰረት የቫናዲየም (V) ምሳሌን በመጠቀም የኬሚካል ንጥረ ነገሮችን ባህሪያት ግምት ውስጥ ያስገቡ-
1. ቪ - ቫናዲየም.
2. መደበኛ ቁጥር - 23. ኤለመንቱ በ 4 ኛ ክፍለ ጊዜ, በ V ቡድን, A (ዋና) ንዑስ ቡድን ውስጥ ነው.
3. Z=23 (የኑክሌር ክፍያ)፣ M=51 (የጅምላ ቁጥር)፣ e=23 (የኤሌክትሮኖች ብዛት)፣ p=23 (የፕሮቶን ብዛት)፣ n=51-23=28 (የኒውትሮን ብዛት)።
4. 23 V 1s 2 2s 2 2p 6 3s 2 3p 6 3d 3 4s 2 - ኤሌክትሮኒክስ ውቅር፣ ቫልንስ ኤሌክትሮኖች 3d 3 4s 2
5. መሰረታዊ ሁኔታ
አስደሳች ሁኔታ

6. ዲ-ኤለመንት, ብረት.
7. ከፍተኛው ኦክሳይድ - V 2 O 5 - የአምፊቶሪክ ባህሪያትን ያሳያል, የአሲድ የበላይነት;
V 2 O 5 + 2NaOH \u003d 2NaVO 3 + H 2 O
V 2 O 5 + H 2 SO 4 \u003d (VO 2) 2 SO 4 + H 2 O (pH)<3)
ቫናዲየም የሚከተሉትን ጥንቅር V (OH) 2, V (OH) 3, VO (OH) 2 ሃይድሮክሳይድ ይፈጥራል. V(OH) 2 እና V(OH) 3 በመሰረታዊ ባህሪያት ተለይተው ይታወቃሉ (1፣ 2) እና VO(OH) 2 አምፊተሪክ ባህሪይ አለው (3፣ 4)።
V (OH) 2 + H 2 SO 4 \u003d VSO 4 + 2H 2 O (1)
2 ቮ (ኦኤች) 3 + 3 ሸ 2 SO 4 \u003d V 2 (SO 4) 3 + 6 H 2 O (2)
VO(OH) 2 + H 2 SO 4 = VOSO 4 + 2 H 2 O (3)
4 VO (OH) 2 + 2KOH \u003d K 2 + 5 H 2 O (4)
8. አነስተኛ የኦክሳይድ ሁኔታ "+2", ከፍተኛ - "+5"
የችግር አፈታት ምሳሌዎች
ምሳሌ 1
| ተግባሩ | የኬሚካል ንጥረ ነገር ፎስፎረስ ይግለጹ |
| መፍትሄ | 1. ፒ - ፎስፎረስ. 2. መደበኛ ቁጥር - 15. ኤለመንቱ በ 3 ኛ ክፍለ ጊዜ, በ V ቡድን, A (ዋና) ንዑስ ቡድን ውስጥ ነው. 3. Z=15 (የኑክሌር ክፍያ)፣ M=31 (የጅምላ ቁጥር)፣ e=15 (የኤሌክትሮኖች ብዛት)፣ p=15 (የፕሮቶን ብዛት)፣ n=31-15=16 (የኒውትሮን ብዛት)። 4. 15 P 1s 2 2s 2 2p 6 3s 2 3p 3 - የኤሌክትሮኒካዊ ውቅር, ቫልንስ ኤሌክትሮኖች 3s 2 3p 3. 5. መሰረታዊ ሁኔታ አስደሳች ሁኔታ 6. p-element, ብረት ያልሆነ. 7. ከፍተኛው ኦክሳይድ - P 2 O 5 - የአሲድ ባህሪያትን ያሳያል. P 2 O 5 + 3Na 2 O \u003d 2Na 3 PO 4 ከከፍተኛው ኦክሳይድ ጋር የሚዛመደው ሃይድሮክሳይድ - H 3 PO 4, የአሲድ ባህሪያትን ያሳያል. ሸ 3 ፖፖ 4 + 3 ናኦህ \u003d ና 3 ፖ 4 + 3ህ 2 ኦ 8. ዝቅተኛው የኦክሳይድ ሁኔታ "-3" ነው, ከፍተኛው "+5" ነው. |
ምሳሌ 2
| ተግባሩ | የኬሚካል ንጥረ ነገር ፖታስየምን ይግለጹ |
| መፍትሄ | 1. K - ፖታስየም. 2. መደበኛ ቁጥር - 19. ኤለመንቱ በጊዜ 4, በቡድን I, A (ዋና) ንዑስ ቡድን ውስጥ ነው. |


